4 次の35問題のうち25問題を選択して解答せよ。(解答欄に1つだけマークすること。)
4-1 アミンの塩基性を水中25℃で測定したとき、次のうち最も塩基性の強いものはどれか。
(1) アニリン
(2) p-メチルアニリン(p-トルイジン)
(3) p-クロロアニリン
(4) p-メトキシアニリン(p-アニシジン)
(5) p-ニトロアニリン
| 速星さんの解説 |
パラ位に電子供与性基が置換すると、アミンの塩基性が強くなります。
これは、アミンの共役酸であるアンモニウムの正電荷の非局在化の程度が、パラ位からの電子押し出しによって、より大きくなるためです。
電子供与性の程度は、メトキシ>メチル>(無置換)>クロロ>ニトロ |
4-2 分子式C7H16で示された鎖状アルカンには、いくつの異性体が存在するか、次の中から選べ。
(1) 8
(2) 9
(3) 10
(4) 11
(5) 12
| 速星さんの解説 |
問題文中には単に「異性体」と書かれており、どの異性体まで含むのか微妙なところですが、構造・幾何・立体の各異性体を指すものと解釈するのが無難でしょう。ただし本問では、直鎖アルカンが対象ですので、幾何異性体は存在しません。
構造異性体は以下の9種類です。
主鎖がC7:n-ヘプタン
主鎖がC6:2-メチルヘキサン(*)
主鎖がC5:2,2-ジメチルペンタン、2,3-ジメチルペンタン(*)、2,4-ジメチルペンタン、3,3-ジメチルペンタン、3-エチルペンタン
主鎖がC4:2,2,3-トリメチルブタン
このうち、(*)を付した2つの構造異性体には、それぞれ光学異性体が存在します。
従って、合計11種類の異性体が存在します。 |
4-3 核磁気共鳴分光法に関する次の記述のうち、正しいものはどれか。
(1) 核磁気共鳴分光法は、原子核近傍の電子を観測する方法である。
(2) 1Hと2Hはどちらも核磁気共鳴分光法で観測できるが、12Cと13Cでは前者しか観測できない。
(3) プロトン核磁気共鳴分光法の積分値は、各ピークに由来する水素の絶対数を示している。
(4) プロトン核磁気共鳴分光法において、エタノールのメチル基由来の水素は、四重線として観測される。
(5) プロトン核磁気共鳴分光法において、エチレン(CH2=CH2)は1本のピークしか与えない。
| 速星さんの解説 |
(1) 原子核のスピンの状態を観測する方法です。
(2) 陽子数と中性子数のうち、少なくとも一方が奇数の原子核が観測可能です。12Cは陽子数6、中性子数6であり、両方が偶数なので観測できません。
(3) 積分値は、水素の相対数を示しています。絶対数を決定するには、内部標準物質と積分値を比較したり、他の分析手法と組み合わせる必要があります。
(4) 隣接するメチレン(CH2)とのカップリングにより、三重線として観測されます。
(5) 全ての水素が等価ですので、1本のピークしかみられません。 |
4-4 イソプロピルベンゼン(クメン)を原料とするクメン法は、ある化合物の工業的製法として知られている。この化合物に最も適したものは次のうちどれか。
(1) アニリン
(2) フェノール
(3) 安息香酸
(4) ベンズアルデヒド
(5) トルエン
| 速星さんの解説 |
| ベンゼン+プロピレン → クメン → クメンヒドロペルオキシド → フェノール+アセトン |
4-5 第三級アルコールによる脱水反応に関する次の記述のうち、正しいものはどれか。
(1) 脱離反応の起こりやすさから、より置換度の低いアルケンが生成する。
(2) この脱水反応を進行させるには、触媒量の酸で十分である。
(3) この反応の機構は、E2脱離反応に分類される。
(4) 反応溶媒には、極性の低いヘキサンなどが適している。
(5) この反応は、水酸化物イオン(OH-)の脱離から始まる。
| 速星さんの解説 |
カルボカチオンを経由する、いわゆるE1反応です。
(4) カルボカチオンを安定化できる、極性溶媒が適しています。
(5) OH-は脱離能の低い基です。この反応は、プロトン化によって生じたオキソニウムイオンの脱離によって開始されます。 |
4-6 次の記述の、(a)~(e)に入る語句の正しい組み合わせは(1)~(5)のうちどれか。
代表的なケトンであるシクロヘキサノンは、水素化ホウ素ナトリウムと反応して、(a)に、また(b)で処理してアジピン酸(ヘキサン二酸)へと容易に変換できる。また、ヒドロキシルアミンとシクロヘキサノンの脱水縮合で得られる(c)化合物は、(d)転移反応を経由して、ナイロン6(PA6)の原料である(e)を与えることが知られている。
(1) (a)シクロヘキサノール、(b)二酸化マンガン、(c)オキシム、(d)クライゼン(Claisen)、(e)ε-カプロラクタム
(2) (a)シクロヘキサノール、(b)過マンガン酸カリウム、(c)ヒドラゾン、(d)ベックマン(Beckmann)、(e)ε-カプロラクトン
(3) (a)シクロヘキサノール、(b)過マンガン酸カリウム、(c)オキシム、(d)ベックマン(Beckmann)、(e)ε-カプロラクタム
(4) (a)シクロヘキセノール、(b)過マンガン酸カリウム、(c)ヒドラゾン、(d)クライゼン(Claisen)、(e)ε-カプロラクトン
(5) (a)シクロヘキセノール、(b)二酸化マンガン、(c)ヒドラゾン、(d)ベックマン(Beckmann)、(e)ε-カプロラクタム
| 速星さんの解説 |
(a) ケトンをNaBH4で還元しているので、生成物はアルコールです。
(b) 強酸化剤による酸化開裂反応。工業的には、空気(触媒:酢酸銅/酢酸マンガン)や硝酸が用いられています。
(c)~(e) ナイロン6の代表的な製造工程です。Beckmann転位に代わる手法として、東レが開発した光ニトロソ化法(PNC法)も知っておくとよいでしょう。。 |
4-7 次に挙げるエネルギー源のうち、一次エネルギーでないものはどれか。
(1) 天然ガス
(2) 都市ガス
(3) 水力
(4) 石油・石炭
(5) ウラン(原子力)
| 速星さんの解説 |
| (2) 都市ガスには通常、天然ガスにLPガスを添加して増熱したものが用いられています。 |
4-8 液体石油製品の物理的及び熱力学的諸性質に関して、密度・比重に比例して大きくなるものは次のうちどれか。
(1) 比熱(比熱容量)
(2) 熱伝導率
(3) 蒸発潜熱
(4) 体膨張係数(熱膨張率)
(5) 発熱量(単位体積当たり)
4-9 石油の精製プロセスに関する次の記述のうち、誤っているものはどれか。
(1) 常圧蒸留装置は、原油を常圧にて蒸留し、LPG、ナフサ、灯油、軽油、常圧残油などの各留分に分ける装置である。
(2) 接触改質法で副生する多量の水素は、水素化精製プロセスや製油所内の燃料として用いられる。
(3) 接触分解装置で必要な熱は、触媒上に析出したコークス(コーク)を燃焼再生する際に得られるため、大型の加熱炉は不要である。
(4) 水素化分解法は、軽質ガスや炭素の生成が少なく、原料に対する液状製品の容積収率は120%程度に達することがある。
(5) 重質油の脱硫法には、直接脱硫法と間接脱硫法があり、我が国では直接脱硫法が主流である。
4-10 石油製品に関する次の記述のうち、誤っているものはどれか。
(1) ガソリンのオクタン価は、JISではリサーチ法オクタン価(RON)で表示されている。
(2) 灯油は、煙点が高いほど燃焼性がよい。
(3) 軽油は、セタン価が低いほど着火性がよい。
(4) 重油は、動粘度によって1種(A重油)、2種(B重油)、3種(C重油)に分類されている。
(5) アスファルトは、針入度が小さいほど硬くなる。
| 速星さんの解説 |
| (3) セタン価は自己着火性の尺度。 |
4-11 潤滑油に関する次の記述のうち、誤っているものはどれか。
(1) エンジン油の「SE」や「SF」などの表示は、SAE粘度分類を示したものである。
(2) 船舶用ディーゼルエンジン油では、燃料の硫黄含有量が高いため硫酸中和性が重要である。
(3) タービン油には、酸化防止剤などの添加剤を含まないものがある。
(4) 切削油剤には、不水溶性型と水溶性型がある。
(5) グリースは、チキソトロプックな性質をもっている。
4-12 石炭類に関する次の記述のうち、誤っているものはどれか。
(1) 我が国の石炭炭質区分は、燃料比(固定炭素/揮発分)と発熱量を基準に定められている。
(2) 無煙炭は燃料比が4以上で、非粘結性である。
(3) 瀝青炭は亜瀝青炭より石炭化が進んでおり、粘結性を有する。
(4) 亜炭は、褐炭より石炭化が進んでいるが、発熱量は瀝青炭より低い。
(5) 褐炭は、燃料比が1.5以下で、非粘結性である。
| 速星さんの解説 |
| (4) 石炭化度(燃料比)の順に、無煙炭>瀝青炭>亜瀝青炭>褐炭>亜炭>泥炭。 |
4-13 ポリエチレン(PE)に関する(A)~(E)の記述のうち、誤っているものの組み合わせは(1)~(5)のうちどれか。
(A)チーグラー触媒を用いて低圧下で合成されるものは、結晶化度が高いため密度が大きい。
(B)高圧下、少量の酸素あるいは過酸化物を開始剤とするラジカル重合により得られるものは、低密度PEと呼ばれる。
(C)分岐の多いPEは自由体積が小さいため、分岐の無いものに比べて弾性率が小さい。
(D)高密度PEの分子量を100万以上に上げた超高分子量PEは、通常のPEに比べ強度、耐摩耗性、低温時の耐衝撃性に優れている。
(E)PEは、ポリプロピレンと同様、極性のプラスチックであり、接着剤などと結びつく基を持っていないため、接着しにくく、また印刷しにくいという性質を有している。
(1) A, B (2) A, C (3) B, D (4) C, E (5) D, E
4-14 高分子の化学構造に関する次の記述の、(a)~(e)に入る語句の正しい組み合わせは(1)~(5)のうちどれか。
高分子が非晶性であるか結晶性であるかは、その構造によって支配される場合が多い。
高分子の結晶化の程度は、分子構造の規則性と密接に関係している。 四フッ化エチレン樹脂(PTFE)のように化学構造が規則的なもの、また不斉炭素原子があっても(a)ポリマーや(b)ポリマーのような立体規則性ポリマーは結晶化しやすい。それに対し(c)構造のものは結晶化しにくい。
非晶領域では高分子鎖は結晶領域のように規則正しく配列しておらず、(d)やゴーシュ領域が入り乱れた構造となっているものがある。
(e)領域の存在が高分子の柔軟性、耐疲労性、染色性に深くかかわっている。
a b c d e
(1) シンジオタクチック イソタクチック アタクチック トランス 非晶
(syndiotactic) (isotactic) (atactic) (trans)
(2) イソタクチック シンジオタクチック トランス アタクチック 結晶
(3) イソタクチック アタクチック シンジオタクチック トランス 無定型
(4) シンジオタクチック トランス イソタクチック アタクチック 結晶
(5) アタクチック シンジオタクチック トランス イソタクチック 非晶
| 速星さんの解説 |
(a)~(c) 側鎖の立体配置による分類。
シンジオタクチックポリマー:立体が交互になっているもの。
イソタクチックポリマー:立体が全てそろったもの。
アタクチックポリマー:立体規則性がないもの。 |
4-15 高分子の分子構造に関する次の記述の下線部([ ]で示す)のうち、誤っているものはどれか。
出発原料となる低分子物質には、ビニルモノマー、[(1) 二重結合1個を含むジエンモノマー]、官能基を2個以上もつアミノ酸、ヒドロキシカルボン酸、さらにエチレンオキシドのような[(2) 環状モノマー]がある。
高分子を形成するモノマーが1種類のときは、この高分子をホモポリマーといい、2種類以上のモノマーからできているときは、共重合体あるいは[(3) コポリマー]と呼ぶ。
共重合体のモノマーの配列にはいろいろの種類があり、モノマーの結合順序がランダムのときは、この共重合体をランダム共重合体と呼ぶ。また、モノマーがある規則性を持って結合する場合、例えばAとBというモノマーが共重合するとき、
ABABABAB・・・・・
のようにAとBが交互に結合しているものを[(4) 交互共重合体]、
(AA・・・AA)(BB・・・BB)(AA・・・AA)(・・
のように、ある程度連続してブロック的な配列をとるものを[(5) ブロック共重合体]という。
| 速星さんの解説 |
| (1) ジエンモノマーなのだから当然、二重結合は2個です。なお、ポリマー中のモノマーユニットに残っている二重結合は1個ですので注意しましょう。 |
4-16 次のうち、樹脂とそれを合成するための主原料の組合せとして誤っているものはどれか。
(1) (樹脂)ポリアセタール樹脂、(主原料)アジピン酸、ヘキサメチレンジアミン
(2) (樹脂)エポキシ樹脂、(主原料)エピクロロヒドリン、多価フェノール
(3) (樹脂)ポリエチレンテレフタレート樹脂、(主原料)テレフタル酸、エチレングリコール
(4) (樹脂)ポリカーボネート樹脂、(主原料)ホスゲン、ビスフェノールA
(5) (樹脂)不飽和ポリエステル樹脂、(主原料)無水フタル酸、無水マレイン酸、エチレングリコール
| 速星さんの解説 |
| (1) ポリアセタール樹脂の主原料はトリオキサン(ホルムアルデヒドの環状3量体)。アジピン酸とヘキサメチレンジアミンから合成される樹脂はナイロン66。 |
4-17 高分子材料の力学モデルに関する次の記述の、(a)~(e)に入る語句の正しい組合せは(1)~(5)のうちどれか。
粘弾性は、材料の力学的挙動がフック弾性的な弾性挙動と、ニュートン粘性的な粘性挙動を同時に示すような挙動である。このとき、弾性をスプリングで、また粘性をダッシュポットで表すとき、両社を(a)に組み合わせたマクスウェル(Maxwell)モデル、(b)に組み合わせたフォークト(Voigt)モデルとがある。マクスウェルモデルは、ひずみ一定の下で応力が時間とともに(c)する現象、すなわち応力緩和を記述することができる。この応力緩和の遅速を特徴づけるのが緩和時間である。一方、フォークトモデルは、応力一定の下でひずみが時間とともに(d)する現象、すなわち(e)を記述することができる。このひずみ変化の遅速を特徴づけるのが遅延時間である。
(1) (a)直列、(b)並列、(c)増加、(d)減少、(e)クリープ
(2) (a)並列、(b)直列、(c)減少、(d)増加、(e)ひずみ硬化
(3) (a)直列、(b)並列、(c)減少、(d)増加、(e)クリープ
(4) (a)並列、(b)直列、(c)減少、(d)増加、(e)降伏現象
(5) (a)直列、(b)並列、(c)増加、(d)減少、(e)チキソトロピー
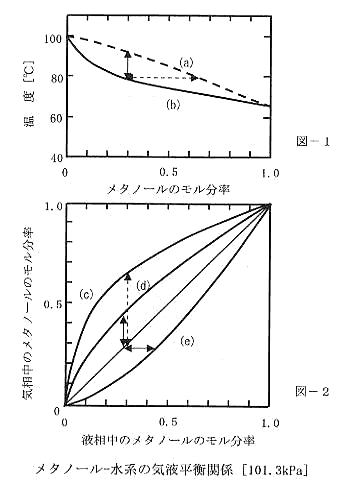
4-18 平衡状態における液相組成―気相組成―温度―圧力の関係を気液平衡図で表すことができる。その一例としてメタノールー水系の気液平衡関係を下図(Fig01)に示す。
次の記述の下線部( [ ]で示す) (ア)~(エ)について、正しいものの組合せは(1)~(5)のうちどれか。ただし、図1、図2においての矢印(実線同士と破線同士)は、それぞれ同じ長さである。
図―1は平衡温度と組成との関係を示す。図中の線(a)は、[(ア)液相線(又は沸点曲線)]を示し、線(b)は、[(イ)気相線(又は露点曲線)]を示す。
メタノールの沸点は、[(ウ)約65℃]である。
図―2は液相組成と気相組成の関係を示したもので、気液組成線図という。図―1から気液組成線図(図―2)を作図すると、[(エ)曲線(c)]が得られる。
(1) (ア), (イ)
(2) (イ), (ウ)
(3) (ア), (エ)
(4) (ウ), (エ)
(5) (イ), (エ)
| 速星さんの解説 |
(ア)~(イ) 液相線と気相線が逆。
(ウ) 図-1において、メタノールのモル分率が1のときの温度は約65℃。
(エ) 80℃におけるメタノールのモル分率は、図-1より、液相で0.3、気相で約0.63。図-2において、液相中のモル分率が0.3のときに、気相中のモル分率が0.63となる気液組成線は、(c)。 |
4-19 熱力学的計算には、圧力、温度、体積、エンタルピー、エントロピーの5つが重要である。
水蒸気の比エンタルピー(h)―比エントロピー(s)線図を下図(Fig02)に示す。
次の記述のうち、誤っているものはどれか。
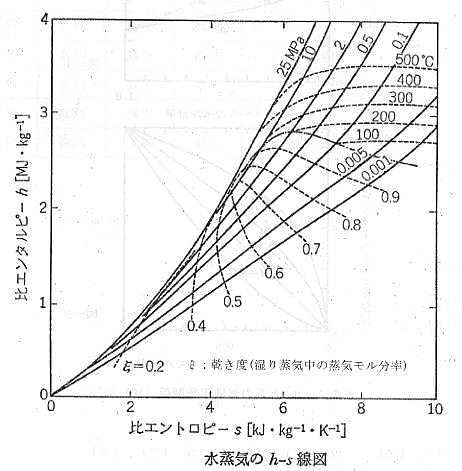
(1) 2MPaでの飽和温度は、おおよそ200℃である。
(2) 0.1MPa、乾き度90%の状態は、100℃の水蒸気90%と100℃の凝縮水10%の混合物である。
(3) 0.5MPa、400℃の水蒸気を0.1MPaまで断熱自由膨張(ジュールートムソン効果)させると、おおよそ100℃となる。
(4) 100℃の飽和蒸気のエンタルピーは、臨界点(374℃、22MPa)のエンタルピーより大きい。
(5) 0.1MPa、100℃の飽和蒸気を0.5MPaまで、圧縮機で昇圧すると乾き蒸気となる。
4-20 ハロゲンに関する次の記述のうち、誤っているものはどれか。
(1) ハロゲン原子は希ガス原子の閉殻電子配置より電子1個だけ少ない電子配置を持ち、きわめて反応性に富む。
(2) フッ化水素酸は強酸で、ガラスを腐食するので、フッ素系高分子容器で取り扱う。
(3) Cl2, Br2及びI2の飽和水溶液では、不均化反応により次亜ハロゲン酸(HXO)を生成する。
(4) 次亜塩素酸HClOは強い酸化作用を示すため、漂白剤や殺菌剤として用いられる。
(5) 塩素酸カリウムKClO3などのハロゲン酸塩は、有機物などが混在していると加熱や衝撃により爆発しやすい。
| 速星さんの解説 |
(2) フッ化水素酸は弱酸。
(3) X2+H2O=HX+HXO
(4) 水道水やプールの水の殺菌剤として、広く用いられている。 |
4-21 水素に関する次の記述のうち、誤っているものはどれか。
(1) 最近の我が国における水素の工業的製造は水の電気分解が主流である。
(2) 水素は、非常に高い電気陽性の性質を持つ金属と反応する場合は負イオンとなる。
(3) 水素には、軽水素:1H、重水素2H(ジュウテリウム:D)、三重水素3H(トリチウム:T)の質量数の異なる3種の同位体が存在する。
(4) 重水は、水を電気分解すると残部にやや多く残る特性を利用して、水の電気分解を繰り返してつくる。
(5) アンモニアを合成するハーバー・ボッシュ法では、水素を大量にリサイクル使用する。
4-22 ガラスに関する次の記述のうち、誤っているものはどれか。
(1) 鉛ガラスは主成分の1つにPbOを含み、放射線防護ガラスや高屈折、高級装飾品用のフリントガラス、クリスタルガラス等に使用される。
(2) 板ガラスを軟化点近くまで熱し、空気を吹きつけて一様に急令すると、表面に均一な圧縮応力が生じ、強度がが向上する。これが強化ガラスで、自動車のフロントガラスに用いられる。
(3) Na2O―B2O3―SiO2系ホウ酸塩のガラスの加熱処理による分相と酸処理などによって多孔質ガラスが得られ、触媒担体や高温気体の分離膜等に使われる。
(4) 結晶化ガラスは他のガラスに比べて線膨張係数が大きいので、直火用調理器具などに適する。
(5) 光ファイバー用シリカガラス製法として、液体SiO4を原料とした化学気相析出(CVD)法がある。
| 速星さんの解説 |
| (4) ガラスが直火加熱で割れやすいのは、部分的な熱膨張で歪みが出るから。従って、線膨張係数が小さいものが加熱用途に適しています。 |
4-23 シリコン系の半導体に関する次の記述の、(a)~(e)に入る語句の正しい組合せは(1)~(5)のうちどれか。
純粋なシリコン単結晶に不純物として微量のPを添加すると、不純物からの余分な(a)が導電性に寄与する(b)半導体となり、ホウ素の微量添加で、(c)半導体になる。アモルファスシリコンは(d)で製造され、(e)アモルファスシリコンであり、pn接合半導体として使用されている。
(1) (a)電子, (b)p型, (c)n型, (d) チョクラルスキー法(引き上げ法), (e)純粋な
(2) (a)正孔, (b)p型, (c) n型, (d)グロー放電による熱分解, (e)水素化
(3) (a)正孔, (b)n型, (c) p型, (d)グロー放電による熱分解, (e)純粋な
(4) (a)電子, (b) n型, (c) p型, (d)グロー放電による熱分解, (e)水素化
(5) (a)電子, (b) n型, (c) p型, (d) チョクラルスキー法(引き上げ法), (e)純粋な
4-24 次の電池のうち、二次電池でないものはどれか。
(1) 鉛蓄電池
(2) ニッケルーカドミウム電池
(3) ニッケルー金属水素化物電池
(4) リチウムイオン電池
(5) 燃料電池
| 速星さんの解説 |
| 二次電池とは、充電可能な電池のこと。 |
4-25 炭素繊維強化複合材料に使われる炭素繊維に関する次の記述のうち、誤っているものはどれか。
(1) 炭素繊維はグラファイト微結晶の集合体から成り、炭化温度が高いほどグラファイト結晶の成長が著しく、配向度が増し弾性率が高くなる。
(2) レーヨン、ピッチ、PAN(ポリアクリロニトリル)を原料とする商業用炭素繊維には、作り方によって種々のグレードのものがあるが、弾性率が最大のものはPAN系繊維で得られている。
(3) ピッチ系炭素繊維には等方性ピッチとメソフェーズピッチがあり、後者は液相のピッチと固相の中間層を意味するメソフェーズが生成している段階で紡糸・耐炎化処理して得られる。
(4) ピッチ系炭素繊維、PAN系炭素繊維いずれも、高弾性率グレードの弾性率の値は、ガラス繊維強化プラスチックに使用されるガラス繊維よりも大きい。
(5) レーヨンから焼成された炭素繊維は低強度・低弾性率であり、炭素繊維強化プラスチックとしては使用されないが、炭素繊維強化炭素複合材料(C/Cコンポジット)の強化材に用いられる。
4-26 原子量12.011の炭素の安定同位体には、中性子を6つ持つものと7つ持つものがある。このとき、中性子を6つ持つものの割合はどれだけか。次の中から選らべ。
(1) 98.8%
(2) 98.9%
(3) 99.0%
(4) 99.1%
(5) 99.2%
| 速星さんの解説 |
12Cの存在比をxとおけば、
12.011=12×x+13×(1-x)
これを解いて、x=0.989 |
4-27 分子量1万、5万、10万の高分子の質量分率がそれぞれ0.1, 0.4, 0.5で存在する混合系がある。この高分子の数平均分子量は、次のうちどの範囲にあるか。
(1) 10,000~20,000
(2) 20,001~35,000
(3) 35,001~50,000
(4) 50,001~65,000
(5) 65,001~80,000
| 速星さんの解説 |
各分子量の高分子のモル分率は、
(0.1/10000):(0.4/50000):(0.5/100000)=10:8:5
数平均分子量は、
{(10000×10)+(50000×8)+(100000×5)}/(10+8+5)=4.35×10^4 |
4-28 酸素不足の状態で黒鉛40gを全て燃焼させたところ、一酸化炭素80mol%と二酸化炭素20mol%の混合ガスが得られた。この燃焼で発生した熱量は、次のどの値に最も近いか。
ただし、(1)および(2)の熱化学方程式を用いよ。
C(黒鉛) + 1/2O2(気) = CO(気) + 111kJ/mol
CO(気) + 1/2O2(気) = CO2(気) + 283kJ/mol
(1) 145kJ
(2) 170kJ
(3) 250kJ
(4) 485kJ
(5) 560kJ
| 速星さんの解説 |
(1)式と(2)式の両辺をそれぞれ足して、
C(黒鉛)+O2(気)=CO2(気)+394 kJ/mol ……(3)
黒鉛40gは 40/12=3.33 mol
(1)式の反応が80mol%、(3)式の反応が20mol%進行したので、発生した熱量は
111×(3.33×0.80)+394×(3.33×0.20)=558.1 kJ |
4-29 一酸化炭素と水蒸気を反応させて、二酸化炭素と水素を得る反応がある。
いま、一酸化炭素20mol%、水蒸気60mol%、窒素20mol%、水素0mol%、二酸化炭素0mol%からなる混合ガスを100kmol/hの割合で反応管に通し、平衡に達するまで反応させた。反応平衡定数K = 1.0であるとき、一酸化炭素の平衡転化率は、(1)~(5)のうちどの値に最も近いか。
ただし、この気体は理想気体の法則に従い、平衡定数は次式で定義される。
K = (pCO2 × pH2)/(pCO × pH2O)
pCO2, pH2, pCO, pH2Oは、ガスの分圧を示す。
(1) 25%
(2) 35%
(3) 50%
(4) 75%
(5) 95%
| 速星さんの解説 |
CO+H2O=CO2+H2
仕込み時の分圧の比は、
pCO2:pH2O=1:3
COの平衡転化率をxとおけば、平衡定数の式は、
1.0=x・x/(1-x)(3-x)
これを解いて、x=0.75 |
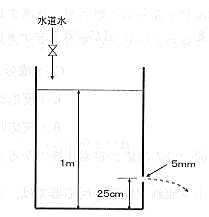
4-30 水の入った円筒形の容器の側面に、底から25cmの位置に直径5mmの孔があけてある。水の水位は底から1mとなるよう、水道水の流量を調整している。このとき孔から放出される単位時間当たりの水の流量は、(1)~(5)のうちどの値に近いか。
尚、次の公式を参考にしてよい。(Fig03)
ベルヌーイの定理:
u2/2g + Z + P/ρg = 一定
P:圧力、g:重力の加速度、z:高さ(距離)、u:流速、ρ:密度
(1) 30L/h
(2) 75L/h
(3) 160L/h
(4) 270L/h
(5) 310L/h
4-31 地球温暖化防止のためには、石炭より天然ガスの方がCO2の発生量が少ないので、熱利用する場合、天然ガスを使う傾向にある。
同じ熱量を得るのに、石炭を燃料とするときに発生するCO2量は、天然ガスを用いたときに発生するCO2量のおおよそ何倍になるか。(1)~(5)から選べ。
石炭を炭素(C)とし、天然ガスはメタン(CH4)として計算せよ。それぞれの生成熱は以下とする。
(成分) CH4、(生成熱ΔHf [kJ/mol]) -74.8
(成分) C、(生成熱ΔHf [kJ/mol]) 0.0
(成分) O2、(生成熱ΔHf [kJ/mol]) 0.0
(成分) CO2、(生成熱ΔHf [kJ/mol]) -393.1
(成分) H2O(g)、(生成熱ΔHf [kJ/mol]) ?241.6
(1) 1.0倍
(2) 1.5倍
(3) 2.0倍
(4) 2.5倍
(5) 3.0倍
| 速星さんの解説 |
表中の生成熱の値を式で表すと、以下のようになります。
C+2H2=CH4+74.8 kJ/mol ……(1)
C+O2=CO2+393.1 kJ/mol ……(2)
H2+1/2O2=H2O(g)+241.6 kJ/mol ……(3)
-(1)+(2)+2×(3) より、
CH4+2O2=CO2+2H2O(g)+801.5 kJ/mol ……(4)
燃焼熱1kJあたりの熱量は、
石炭(C)の場合、(2)式より、
1/393.1=2.54×10^-3 mol/kJ
天然ガス(CH4)の場合、(4)式より、
1/801.5=1.25×10^-3 mol/kJ
従って、求める比率は
(2.54×10^-3)/(1.25×10^-3)=2.03 倍 |
4-32 A→Bの反応は、発熱的に進行する液相均一反応であり、反応速度は成分Aの濃度の一次として、次式のように表される。
反応式 A → B(発熱反応)
反応速度 r = dCA/dθ = -kCA
CA:成分Aの濃度、k:反応速度定数、θ:反応時間
図―1)、図―2)(Fig04)の反応が定常状態であるとき、以下の記述で誤っているものはどれか。
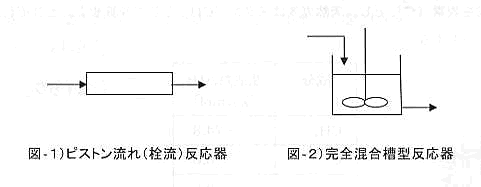
(1) ピストン流れ(栓流)反応器では、成分Aの濃度は、入口から出口に向って減少する。
(2) ピストン流れ(栓流)反応器では、入口付近の除熱量を大きくしないと均一な温度とならない。
(3) 完全混合槽型反応器では、反応器内の成分Aの濃度は出口濃度と同じである。
(4) 完全混合槽型反応器では、混合が十分であれば、槽内の温度を均一に保つことができる。
(5) 完全混合槽型反応器では、槽内の成分Aの濃度を均一にできるので、同じ反応率を得るには、ピストン流れ(栓流)反応器より小さな容積でよい。
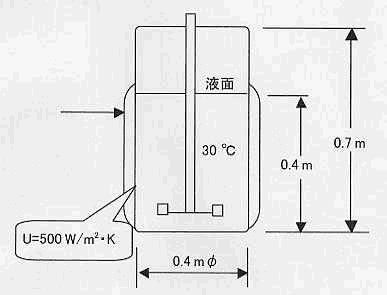
4-33 内径0.4m、深さ0.7m、壁厚さ10mmのジャケット付き攪拌槽に深さ0.4mまで溶液を入れ、110℃の飽和水蒸気をジャケットに通して加熱する。ただし、ジャケットは側面のみに付いている。(Fig05)
溶液は十分攪拌されているので温度は一様であり、攪拌槽内溶液温度は30℃である。総括伝熱係数(U)が500W/m2・Kであるとき、時間当たりの入熱量は、次のどの値に最も近いか。 ただし、1W = 1J/sとする。
(1) 5,600kJ/h
(2) 7,200kJ/h
(3) 72,000kJ/h
(4) 99,000kJ/h
(5) 130,000kJ/h
| 速星さんの解説 |
伝熱面は液面より下なので、その面積は
(π×0.4)×0.4=0.503 m^3
時間当たりの入熱量Qは、
Q=U・S・ΔT
=500×0.503×(110-30)
=2.01×10^4 W
=20.1 kJ/sec
=7.24×10^4 kJ/h |
4-34 結晶水47.3%(質量パーセント)を含むNaxByOz・nH2Oの分析結果は、ナトリウム12.1%、ホウ素11.3%であった。この無水塩中のB:Oの原子数比は、次のうちどれに最も近いか。ただし、Na = 23, B = 10.8, O = 16, H = 1とする。
(1) 10:7
(2) 5:7
(3) 4:7
(4) 2:5
(5) 2:7
| 速星さんの解説 |
質量比は、
Na:B:O:H2O=12.1:11.3:(100-12.1-11.3-47.3):47.3
=12.1:11.3:29.3:47.3
これをmol比に直すと、
Na:B:O:H2O=(12.1/23):(11.3/10.8):(29.3/16):(47.3/18)
=1:1.989:3.481:4.996
≒2:4:7:10
すなわち、はじめの塩の組成は Na2B4O7・10H2O |
4-35 ある温度におけるAgClの飽和水溶液の溶解度積は1×10^(-10)mol2/L2である。この温度で飽和水溶液中のAg+の濃度を1/10にするためには、飽和水溶液1L当たり加えるKCl量は次のうちどれに最も近いか。
(1) 1mol
(2) 0.1mol
(3) 0.01mol
(4) 0.001mol
(5) 0.0001mol
| 速星さんの解説 |
はじめの飽和水溶液中の各塩の濃度は
[Ag+]0=[Cl-]0=1×10^-5 mol/L
KCl添加後のAg+濃度は 1×10^-6 mol/L なので
[Cl-]=Ksp/[Ag+]
=(1×10^-10)/(1×10^-6)
=1×10^-4 mol/L
従って、飽和水溶液 1L あたりのKCl添加量は
([Cl-]-[Cl-]0)×1=0.9×10^-4 mol |
| 正解 |
| 問題 |
正解 |
|
問題 |
正解 |
|
問題 |
正解 |
|
問題 |
正解 |
|
問題 |
正解 |
|
問題 |
正解 |
|
問題 |
正解 |
| 1 |
4 |
|
6 |
3 |
|
11 |
1 |
|
16 |
1 |
|
21 |
1 |
|
26 |
2 |
|
31 |
3 |
| 2 |
4 |
|
7 |
2 |
|
12 |
4 |
|
17 |
3 |
|
22 |
4 |
|
27 |
3 |
|
32 |
5 |
| 3 |
5 |
|
8 |
5 |
|
13 |
4 |
|
18 |
4 |
|
23 |
4 |
|
28 |
5 |
|
33 |
3 |
| 4 |
2 |
|
9 |
5 |
|
14 |
1 |
|
19 |
3 |
|
24 |
5 |
|
29 |
4 |
|
34 |
3 |
| 5 |
2 |
|
10 |
3 |
|
15 |
1 |
|
20 |
2 |
|
25 |
2 |
|
30 |
4 |
|
35 |
5 |




